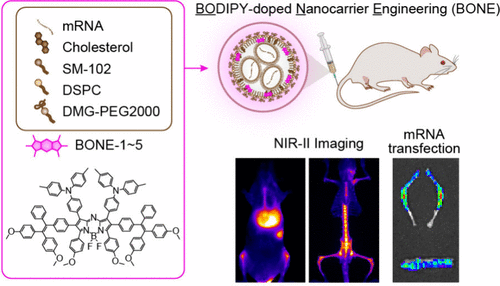
【JACS】提升3.3倍转染效率!科学家给mRNA装上“北斗导航”,直攻深层骨髓堡垒
✨文章标题:BODIPY-Doped Nanocarrier Engineering (BONE) Improves Bone Marrow mRNA Delivery by NIR-II Bioimaging Guided Screening ✉️作者:Mengyao Zhao* Xiaoyuan Chen* 等 🔗链接:https://doi.org/10.1021/jacs.5c14271
[!note]
核心痛点: 骨髓是免疫和造血的核心,但由于血流灌注低和“血-骨髓屏障”的存在,mRNA 极难精准递送至此。传统的骨靶向主要靠结合骨矿物质(如羟基磷灰石),很难进入骨髓内部。
创新策略(BONE): 研究者将具有骨髓亲和力且具备 NIR-II(近红外二区) 发光特性的 Aza-BODIPY 染料,像“导航插件”一样掺杂进经典的脂质纳米颗粒(LNP)中。
双重功能: 这些染料既是示踪剂(实现深层组织非侵入式实时成像,告别“盲盒式”筛选),又是功能成分(通过调节纳米颗粒与细胞的相互作用,改变分布)。
关键结果: * 通过成像筛选出最优配方 BONE-2 LNP,其在骨骼中的富集显著。
效率飞跃: 相比商业化 LNP(Moderna 配方),BONE-2 将骨髓 mRNA 的转染效率提升了 3.3 倍。
细胞精准定位: 这种提升主要发生在髓系细胞(单核、巨噬、树突状细胞)和造血干细胞中,而对淋巴细胞影响较小。
科学意义: 建立了一个“可视化、可筛选、高效率”的通用平台,为白血病、骨髓纤维化等疾病的基因治疗开启了新大门。
骨髓,这个深藏在坚硬骨骼内部的“生命摇篮”,是人体造血和免疫调节的核心枢纽 。然而,在现代基因治疗的版图中,骨髓却是一块极难啃下的“硬骨头” 。
无论是白血病、再生障碍性贫血,还是癌症的骨转移,许多致命疾病的根源都潜伏在骨髓之中 。如果我们能将mRNA——这种能指挥细胞合成特定蛋白质的“生命指令”——精准地送入骨髓,就有可能从源头上修复受损的免疫系统或摧毁癌细胞 。
但现实很残酷。骨髓不仅被厚厚的骨质包围,还存在着极其严苛的“血-骨髓屏障”,加之骨组织的血流灌注率极低,常规的递送系统(如脂质纳米颗粒,LNP)大多在肝脏或脾脏就被拦截了,很难到达这个深层堡垒 。
近日,一项发表在国际化学顶级期刊 《美国化学会志》(JACS) 上的研究,为这一难题带来了突破性的解决方案 。来自复旦大学等机构的研究团队开发了一种名为 BONE 的全新策略,利用近红外二区(NIR-II)生物成像技术,不仅给mRNA递送载体装上了“导航仪”,更将其在骨髓中的转染效率提升了整整 3.3倍 。
一、 核心痛点:为什么骨髓递送总是“石沉大海”?
要理解这项研究的了不起之处,我们得先看看以前的科学家是怎么做的。 过去,为了让药物“粘”在骨头上,最常用的策略是给载体挂上双膦酸盐等基团 。这种方法就像给纳米颗粒装上了磁铁,让它们能够紧紧吸附在骨表面的矿物质(羟基磷灰石)上 。
但问题也随之而来:吸附在骨头表面,并不等于进入了骨髓内部 。这就好比你把快递投递到了小区大门口的保安室,但收件人其实住在地下三层的深处,快递员依然无法“最后一公里”的精准送达 。
更糟糕的是,科学家在筛选这些递送载体时,往往处于“半盲目”状态 。传统的方法主要靠体外模拟实验,或者在动物实验结束后将骨头切碎了检测 。这种方法缺乏实时反馈,无法观察到药物在生物体内流动的真实轨迹,导致筛选效率极低,且容易产生误导性的结果 。
二、 科技破局:NIR-II“透明成像”与BONE导航系统
针对这些挑战,研究团队提出了一种名为 BODIPY掺杂纳米载体工程(BONE) 的策略 。这套系统的核心在于一种经过特殊设计的“功能插件”——Aza-BODIPY染料 。
1. 赋予纳米载体“穿透视力”
这种染料最神奇的地方在于它能发射出 NIR-II(近红外二区,1000-1700 nm) 的荧光 。
我们可以把普通的可见光成像想象成在迷雾中看手电筒,光线会被皮肤和组织散射得模糊不清 。而 NIR-II 窗口 则被称为生物组织的“透明窗口”,光线具有极强的穿透力,可以清晰地穿透深层肌肉和骨骼 。
通过将这种染料掺入 LNP 载体中,研究者就像给每一个纳米颗粒安装了一个微型的“北斗导航终端”,可以在不解剖小鼠的情况下,实时、无创地看到这些颗粒是否真的进入了骨髓 。
2. 从“追踪者”到“引导者”
研究团队合成了一个包含五种不同结构的染料库(BONE-1 到 BONE-5) 。他们惊讶地发现,这些染料不仅能发光,其分子结构本身就能改变 LNP 在体内的“朋友圈” 。
具体来说,这些染料分子会调节纳米颗粒与生物膜及细胞的相互作用 。通过 NIR-II 荧光筛选,研究人员发现 BONE-2 这种特定结构的染料展现出了惊人的“骨髓趋化性” 。 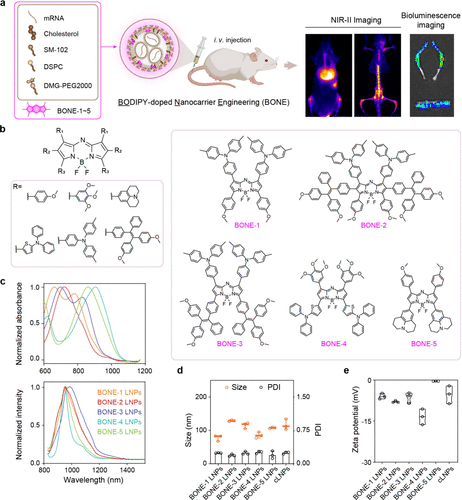
图1: 展示 BONE LNPs 的制备流程及 NIR-II 成像引导下的筛选机制 。
三、 结果分析:数据证明,它真的能深入“生命摇篮”
为了验证 BONE 系统的威力,研究团队进行了一系列严谨的实验对比。他们将掺杂了不同染料的 BONE LNPs 注射进小鼠体内,并与目前最先进的商业化 LNP(Moderna 配方)进行正面对决 。
1. 实时捕获骨髓中的“星光”
在 NIR-II 荧光相机的镜头下,奇迹发生了。注射 24 小时后,原本在常规成像中难以观测的骨骼区域竟然“亮”了起来 。
全方位成像: 无论是胸骨、股骨、胫骨,还是深层的脊柱和骨盆,在 BONE-2 组的小鼠身上都清晰可见 。
高信噪比: 实验数据显示,BONE-2 在后肢的信号背景比(SBR)达到了 10.4,在胸骨达到了 3.4,这是其他配方难以企及的高度 。
更重要的是,研究者将骨头取出并冲洗掉骨髓后发现,超过 70% 的荧光信号消失了 。这有力地证明了纳米颗粒确实是进入了骨髓腔内部,而不是仅仅粘在表面的骨质上 。 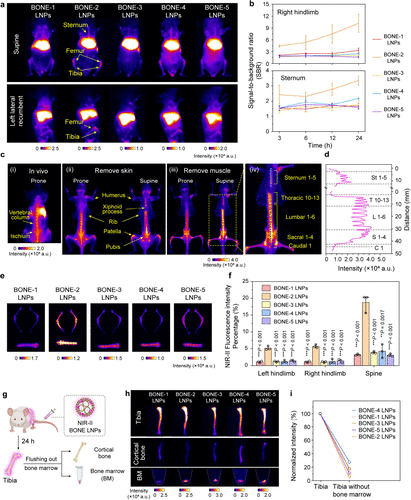
图2: 活体 NIR-II 成像对比及骨髓冲洗前后的定量分析,证明 BONE-2 的骨髓靶向性 。
2. 3.3倍的转染飞跃:让 mRNA 真正“动起来”
成像只是第一步,mRNA 能否在骨髓细胞里成功表达出蛋白质,才是衡量递送效率的金标准 。
研究团队将编码**萤火虫荧光素酶(Fluc)**的 mRNA 装入载体 。这种 mRNA 只要进入细胞并开始工作,就会产生能发光的蛋白质 。
数据对比: 相比于没有“导航”的商业化 LNP(cLNP),BONE-2 LNP 在脊柱区域产生的蛋白表达量足足提升了 3.3 倍 。
广泛适用: 研究者还将该策略应用到了 ALC-0315(辉瑞疫苗同款脂质)等多个临床验证过的递送平台上,均观察到了稳定的骨靶向效果,证明了该策略的通用性 。
3. 精准爆破:哪些细胞被“转化”了?
为了进一步深挖,研究者利用流式细胞术解析了骨髓内部的细胞构成 。结果发现,这种提升具有显著的细胞特异性。
髓系细胞的“偏爱”: BONE-2 LNP 极其擅长进入单核细胞、巨噬细胞和树突状细胞(DCs) 。在单核细胞中,携带高载量货物的细胞比例甚至比对照组高出了 57倍 。
造血干细胞的突破: 更令人振奋的是,对于负责产生所有血细胞的“源头”——造血干细胞(HSCs),BONE-2 的转染效率提升了 2.4 倍 。这为通过 mRNA 疗法进行原位骨髓移植或基因纠正提供了可能 。
淋巴细胞的免疫豁免: 相比之下,B细胞和T细胞等淋巴系细胞的转染几乎没有增加 。这种差异化递送有助于降低潜在的免疫副作用 。
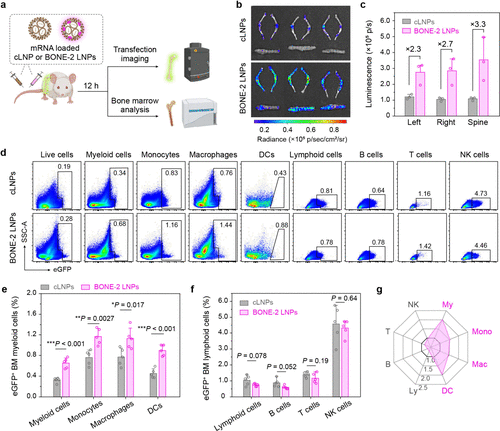
图3: 流式细胞术分析图谱,展示 BONE-2 在髓系细胞和干细胞中的精准分布及 mRNA 表达 。
四、 深度解读:为什么这套“组合拳”能生效?
为什么仅仅掺杂了一点特殊的染料,LNP 的行为就发生了翻天覆地的变化?研究团队通过血液动力学和细胞实验解开了谜团 。
他们发现,BONE-2 分子的加入,显著增强了载体与外周血单核细胞(PBMCs) 的相互作用 。实验显示,BONE-2 在 PBMC 部分的定位信号比 cLNP 高出 8.6 倍 。
这引出了一个巧妙的“特洛伊木马”机制:这些纳米颗粒在血液中会优先被单核细胞等免疫细胞“捕获”,然后随着这些细胞的自然归巢(Homing)行为,像搭乘班车一样被带进骨髓深处 。由于单核细胞本身就起源于骨髓且具备穿透屏障的能力,这种“细胞介导的贩运”打破了以往单纯依靠被动扩散的局限 。
五、 总结与展望:开启基因治疗的“骨髓时代”
这项研究的成功,不仅仅是创造了一个高效的 mRNA 载体,更重要的是它展示了一种全新的科研范式:
从“盲目试错”到“视觉引导”: 利用 NIR-II 成像,科学家可以在活体状态下快速筛选数以百计的配方,极大地缩短了研发周期 。
功能化掺杂的巨大潜力: 证明了荧光分子不仅是看客,更可以通过精细的结构设计成为功能组件,调控载体的体内命运 。
潜在应用场景:
血液疾病: 直接向骨髓递送基因矫正指令,治疗镰刀型贫血或白血病 。
免疫增强: 通过转染骨髓中的树突状细胞,开发更强大的癌症疫苗 。
再生医学: 激活骨髓干细胞,加速骨折愈合或缓解骨质疏松。
当然,该项研究仍处于实验室阶段。未来,这种染料在人体内的长期生物安全性、临床转化过程中的成本控制,以及针对不同骨科疾病的普适性,还需要进一步的研究 。
但不可否认,BONE 策略已经为我们照亮了那条通往深层骨骼堡垒的幽长隧道。正如论文通讯作者所言,这种将实时成像与功能改性相结合的框架,将为开发针对特定器官、组织甚至是特定细胞类型的精准递送系统提供通用的样板 。